La chimie dite « bioorthogonale » est une jeune discipline suscitant de nombreux espoirs. Cette chimie hautement sélective et biocompatible permet de réaliser des réactions non naturelles dans les milieux biologiques (sang, intérieur des cellules …) ou encore au sein d'un organisme vivant. Les nouveaux outils chimiques issus de cette discipline ont déjà permis de développer des technologies de ligation puissantes et utiles pour la préparation de bioconjugués à partir de biomolécules et de composés chimiques. En revanche, très peu de réactions de coupure bioorthogonale ont été décrites à ce jour.
Les chimistes du SCBM viennent de découvrir que certains composés, appelés iminosydnones, sont capables de réagir rapidement dans les milieux biologiques avec des alcynes cycliques pour former deux nouveaux produits : l'un provenant de la ligation des deux partenaires réactionnels, l'autre provenant d'une fragmentation d'un des deux partenaires (figure 1).
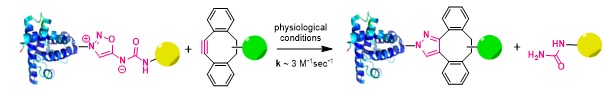
Figure 1 : Réaction de « click and release » entre une protéine portant une iminosydnone et une cyclooctyne. Cette réaction permet de lier un composé chimique (boule verte) à la protéine tout en libérant de celle-ci un autre composé chimique (boule jaune).
En
collaboration avec le SIMOPRO, l’équipe du SCBM a pu démontrer que cette
réaction permettait de marquer et de purifier sélectivement une protéine
présente dans un milieu biologique très complexe (extrait de foie). De plus, un
travail avec l’université de Strasbourg et la société Syndivia a démontré que cette nouvelle réaction pouvait
permettre de décrocher un composé chimique d’un anticorps monoclonal
thérapeutique, ceci de façon quantitative dans le sang.
Ce travail constitue la
première étape d’un projet qui vise à utiliser les outils de la chimie
« bioorthogonale » pour le développement de nouvelles technologies
dans les domaines du marquage, de l’identification des cibles des candidats
médicaments et la libération contrôlée de principes actifs (figure 2).
Les composés chimiques décrits dans cet article ont fait l'objet d'un brevet CEA/CNRS en 2016, brevet que la société Syndivia (dont Frédéric Taran est l'un des membres fondateurs) souhaite exploiter.
Les referees de ce travail l'ont qualifié de « highly important », cette évaluation concernant moins de 10% des articles soumis à Angewandte Chemie Int.Ed.
Ces travaux ont fait l'objet d'une actualité publiée sur le site de la Direction de la recherche fondamentale le 21/12/2017.