Le cuivre est un élément trace essentiel pour l’homme utilisé pour de nombreuses fonctions physiologiques. Etant donné la grande toxicité du cuivre libre, son transport et son stockage sont très finement régulés dans nos cellules. Au cours de la dernière décennie, le cuivre a été montré comme jouant un rôle important dans la tumorigenèse. Différentes thérapies anti-cancéreuses jouant sur le cuivre sont actuellement en cours de développement.
Les chercheurs du CEA-Irig, de l’Institut pour l'Avancée des Biosciences et de l’Université Libre de Bruxelles, ont développé une nouvelle famille de molécules capables de transporter sélectivement à travers une membrane biologique les ions cuivre portant une seule charge positive (Cu⁺) qui correspond à la forme intracellulaire du cuivre [1,2] (Figure a-b). Certains composés de cette famille ont montré une activité anti-cancéreuse sur des cellules en culture. Le Cuphoralix a ainsi été identifié comme la meilleure molécule synthétisée par l’équipe de l’ULB (Figure a) [2,3]. L’expertise des chercheurs du CEA-IRIG sur l’homéostasie du cuivre* a permis d’élucider le mécanisme d’action du Cuphoralix dans des cellules cancéreuses du foie. En collaboration avec des chercheurs du synchrotron ESRF à Grenoble, des expériences de nano-imagerie élémentaire ont montré que le Cuphoralix induit une redistribution du cuivre dans les cellules cancéreuses qui en meurent empoisonnées (Figure c-d).
La sélectivité de molécules comme le Cuphoralix développées pour le transport de Cu+ a permis de découvrir un mécanisme d’action anti-cancéreux totalement inédit. En effet, les mécanismes de résistance développés par les cellules sont très limités puisque le Cuphoralix n’a pas de cible intracellulaire spécifique, ce qui le rend également actif contre tous les types de cellules cancéreuses testés jusqu’à présent : les modèles résistants ou non, et ceux avec ou sans phénotype agressif. Tous ces éléments font du Cuphoralix une molécule très prometteuse pour la thérapie anti-cancéreuse.
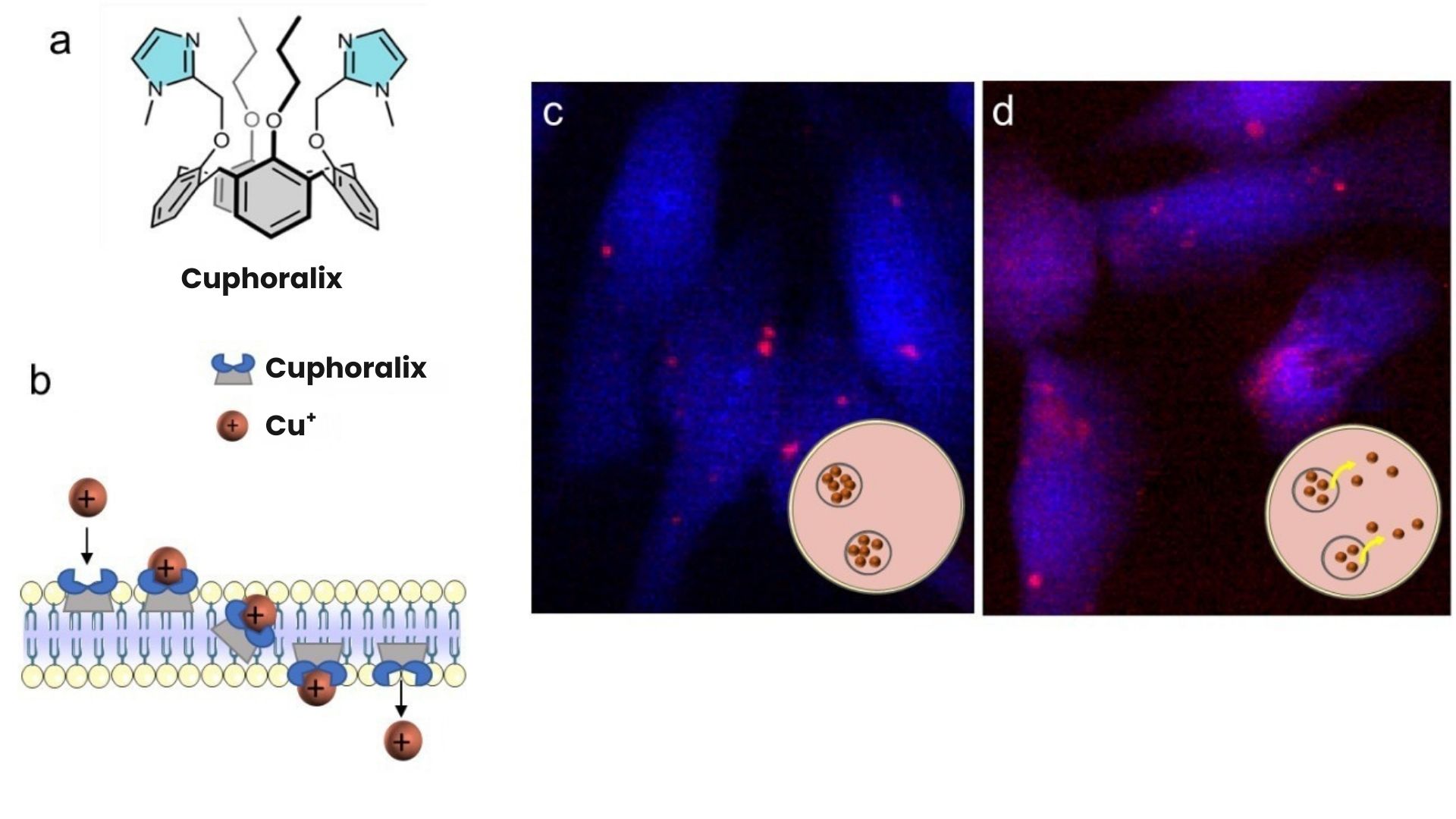
Figure :a) Structure du Cuphoralix.
b) Mécanisme du transport des ions Cu+ à travers une bicouche lipidique par le Cuphoralix.
c-d) Images de microscopie de fluorescence des Rayons X permettant de visualiser la distribution du potassium (bleu) et du cuivre (rouge) dans des cellules de cancer du foie exposées à 10 µM Cu (c) ou à 10 µM Cu et 100 nM Cuphoralix (d).
Ces cartes montrent que le cuivre est physiologiquement stocké à haute concentration dans des vésicules intracellulaires (c, spots rouge intense) et le Cuphoralix empêche ce stockage conduisant à une redistribution du cuivre dans toute la cellule avec des concentrations locales 10 fois plus faibles (d). Les encarts montrent une représentation schématique de la localisation du cuivre dans les cellules.
* L’homéostasie du cuivre correspond à l’ensemble des mécanismes permettant de maintenir la concentration et la distribution intracellulaire du cuivre appropriées.