Aujourd'hui 85% de la demande énergétique mondiale est assurée par les énergies fossiles. La fabrication de nouveaux carburants utilisant des énergies renouvelables et décarbonées s'inscrit dans une optique d'indépendance face aux énergies fossiles. Composé utilisable aussi bien dans les piles à combustible à convertisseur intégré que dans les moteurs à combustion, le méthanol pourrait fournir la clé d'une production de carburant à haute densité énergétique, à partir de ressources renouvelables. Il peut en effet être formé à partir de la réduction à six électrons d'une matière carbonée renouvelable, le CO2. Cependant les catalyseurs existant pour la transformation directe (électrolyse) du CO2 en méthanol ne sont ni efficaces ni sélectifs et l'hydrogénation du CO2 pose des problèmes liés à l'utilisation de hautes pressions. La réduction à deux électrons du CO2 vers l'acide formique est, quant à elle, efficace et bien maîtrisée. Une alternative intéressante pour convertir le CO2 en méthanol serait donc d'utiliser l'acide formique comme relais, à condition d'être ensuite capable de convertir efficacement ce dernier en méthanol.
En 2013, les premiers catalyseurs permettant la conversion de l'acide formique en méthanol voient le jour, avec les travaux du groupe de K. Goldberg à l'université de Washington[2]. Cette avancée repose néanmoins sur l'utilisation d'un métal particulièrement coûteux, l'iridium, et le méthanol n'est obtenu qu'avec un rendement maximum de 2 %. Pour obtenir une approche globale efficace dans l'utilisation du CO2 comme vecteur d'énergie, une meilleure efficacité est donc nécessaire.
[1] Laboratoire de Chimie Moléculaire et Catalyse pour l'Energie (LCMCE)
[2] A. J. M. Miller, D. M. Heinekey, J. M. Mayer, K. I. Goldberg, Angew. Chem. Int. Ed., 2013, 52, 3981.
Aujourd'hui, des équipes de l'Iramis au CEA viennent de développer des catalyseurs efficaces à base de ruthénium transformant l'acide formique en méthanol avec un rendement atteignant 50%. De plus, l'utilisation du ruthénium au lieu de l'iridium présente un avantage économique certain, ce métal étant plus de dix fois moins coûteux que l'iridium. Le mécanisme de la réaction a été étudié par une approche duale, expérimentale et théorique, qui a permis de mettre en évidence les intermédiaires réactionnels et les espèces catalytiques impliqués dans la formation du méthanol. Il a ainsi été montré que l'espèce active en catalyse était un complexe hydrure de ruthénium capable de redistribuer efficacement la liaison C–H de l'acide formique. Cette réaction permet donc de former du méthanol et deux molécules de CO2 à partir de trois molécules d'acide formique. Le bilan carbone total est ainsi favorable puisque trois molécules de CO2 sont nécessaires pour préparer trois molécules d'acide formique.
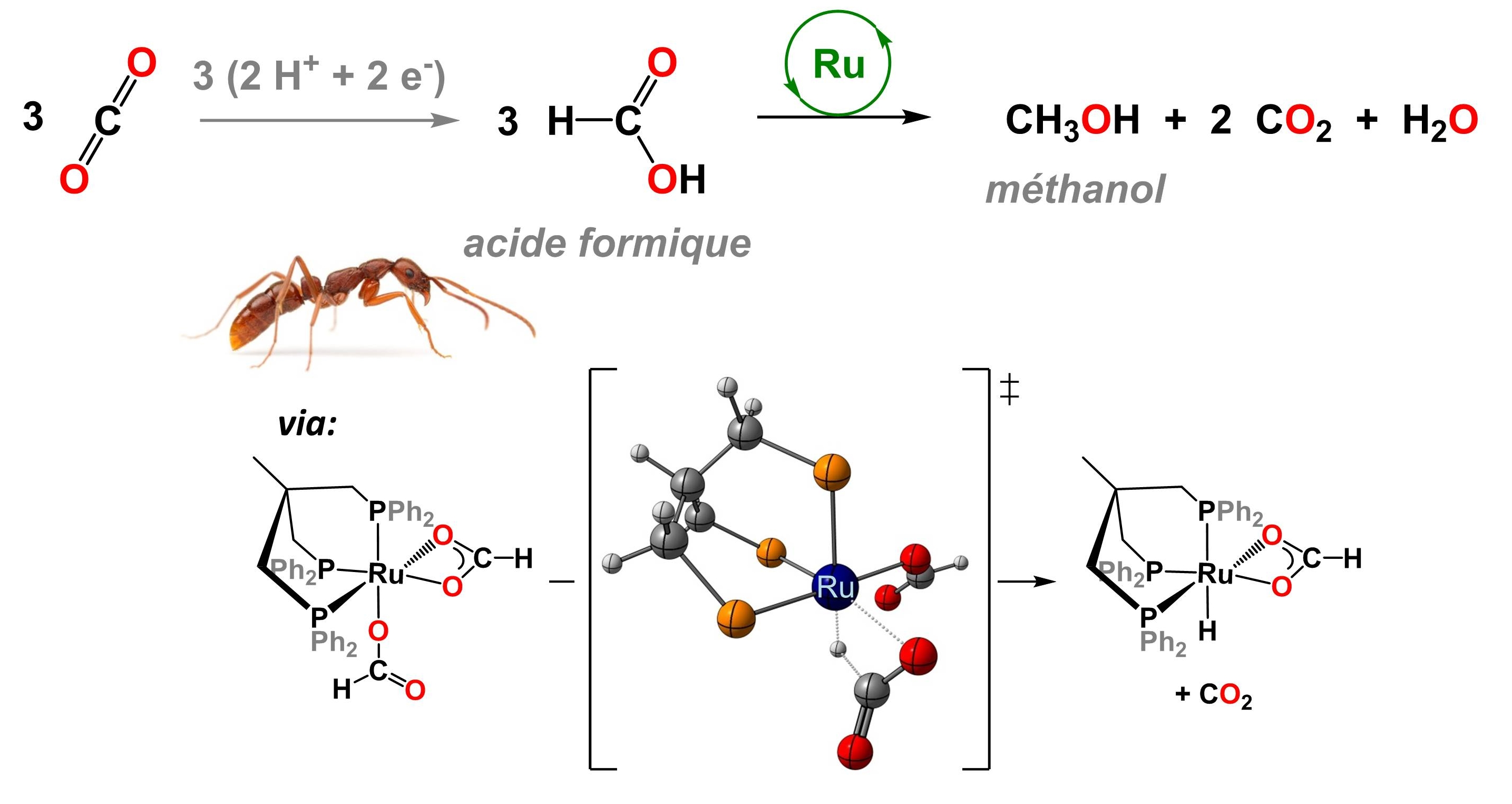
Figure 1. Schéma réactionnel et différents intermédiaires métalliques mis en jeu. CEA
Pour compléter cette approche, les chercheurs envisagent de coupler ces deux réactions pour évaluer le rendement énergétique global de cette nouvelle stratégie de synthèse du méthanol à partir du CO2.